
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- Naposledy změněno 2025-01-22 16:56.
A slabá kyselina disociuje na H+ a jeho konjugát základna , který vytváří vyrovnávací paměť. To odolává změně pH a vyžaduje více základny na neutralizovat to. Přidávání slabá kyselina voda sama o sobě nevytváří nárazník. Takže se to může zdát slabá kyselina potřeby více základny , protože nárůst pH je mnohem pomalejší.
Proč tedy silná kyselina neutralizuje tolik zásady jako slabá kyselina?
Kyselina - Základna Reakce. Když kyseliny an základna reagovat oni neutralizovat navzájem. Silné kyseliny neutralizují silné zásady stejných koncentrací ve stejném množství. Větší objem a slabá kyselina je potřeba neutralizovat A silná základna pokud jsou koncentrace stejné a naopak slabé základy a silné kyseliny.
Podobně, kolik zásady potřebujete k neutralizaci kyseliny? Titrace. Když chlorovodíková kyselina reaguje s hydroxidem sodným, an kyselina / základna molární poměr je 1:1 Požadované za plnou neutralizace . Pokud místo toho chlorovodíková kyselina reagovaly s hydroxidem barnatým v molárním poměru bych být 2:1. Dva moly HCl jsou potřeba úplně neutralizovat jeden mol Ba(OH)2.
Stejně tak se lidé ptají, může silná báze neutralizovat slabou kyselinu?
Když silná kyselina neutralizuje a slabá základna pH výsledného roztoku vůle být menší než 7. Když a silná základna neutralizuje a slabá kyselina pH výsledného roztoku vůle být větší než 7.
Jak neutralizujete slabou bázi?
Použijte a slabý okyselit neutralizovat báze . Příklady zahrnují hydroxid sodný, hydroxid draselný a amoniak. Mnoho různých produktů pomáhá v neutralizace kyselin a základny . Mohou být tak jednoduché jako sáček s kyselinou citronovou nebo seskvikarbonátem sodným, nebo tak složité jako kombinace ztužovače a neutralizátoru.
Doporučuje:
Jak se nazývá sůl vzniklá neutralizací kyseliny chlorovodíkové a hydroxidu sodného?
Vysvětlení: Reakce mezi hydroxidem sodným (NaOH) a kyselinou chlorovodíkovou (HCl) je neutralizační reakce, jejímž výsledkem je tvorba soli, chloridu sodného (NaCl) a vody (H2O). Jde o exotermickou reakci
Přidáváte kyselinu do zásady nebo zásadu do kyseliny?

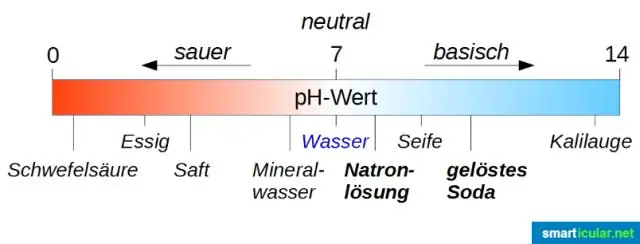
Přidáním kyseliny se zvýší koncentrace iontů H3O+ v roztoku. Přidáním zásady se sníží koncentrace iontů H3O+ v roztoku. Kyselina a zásada jsou jako chemické protiklady. Pokud je do kyselého roztoku přidána báze, roztok se stává méně kyselým a pohybuje se směrem ke středu stupnice pH
Jak určíte množství kyseliny potřebné k neutralizaci zásady?

Řešení problému acidobazické neutralizace Krok 1: Vypočítejte počet molů OH-. Molarita = mol/objem. mol = molarita x objem. mol OH- = 0,02 M/100 mililitrů. Krok 2: Vypočítejte potřebný objem HCl. Molarita = mol/objem. Objem = mol/molarita. Objem = mol H+/0,075 Molarita
Kolik kyseliny je potřeba k neutralizaci báze?

Titrace. Když kyselina chlorovodíková reaguje s hydroxidem sodným, je pro úplnou neutralizaci nutný molární poměr kyselina/báze 1:1. Pokud by místo toho kyselina chlorovodíková reagovala s hydroxidem barnatým, molární poměr by byl 2:1. K úplné neutralizaci jednoho molu Ba(OH)2 jsou zapotřebí dva moly HCl
Jaké jsou slabé kyseliny?

Slabá kyselina je kyselina, která ve vodném roztoku neprodukuje mnoho vodíkových iontů. Slabé kyseliny mají relativně nízké hodnoty pH a používají se k neutralizaci silných zásad. Mezi příklady slabých kyselin patří: kyselina octová (ocet), kyselina mléčná, kyselina citrónová a kyselina fosforečná
