
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- Naposledy změněno 2025-01-22 16:56.
VIDEO
Jak tedy řešíte problémy s atomovou hmotností?
Na vypočítat a atomová hmotnost jednoho atomu prvku, sečtěte Hmotnost protonů a neutronů. Příklad: Najděte atomová hmotnost izotopu uhlíku, který má 7 neutronů. Z periodické tabulky můžete vidět, že uhlík má an atomový číslo 6, což je počet jeho protonů.
Navíc, co je atomové hmotnostní číslo? The hromadné číslo (symbol A, z německého slova Atomgewicht [ atomový hmotnost]), také nazývané atomové hmotnostní číslo nebo nukleon číslo , je celkem číslo protonů a neutronů (společně známých jako nukleony) v an atomový jádro. The hromadné číslo je odlišný pro každý jiný izotop chemického prvku.
Dále je třeba vědět, jaký je vzorec atomové hmotnosti?
Průměrný atomová hmotnost = f1M1 + f2M2 +… + f M kde f je zlomek představující přirozené množství izotopu a M je izotop Hmotnost číslo (hmotnost) izotopu. Průměrný atomová hmotnost prvku lze nalézt v periodické tabulce, obvykle pod symbolem prvku.
Co je průměrná atomová hmotnost v chemii?
The průměrná atomová hmotnost prvku je součet masy jeho izotopů, každý vynásobený jeho přirozeným množstvím (desetinné číslo spojené s procentem atomy tohoto prvku, které jsou daného izotopu).
Doporučuje:
Jak vypočítáte průměrnou atomovou hmotnost stroncia?

Vypočítáme to tak, že vezmeme váženou hmotnost každého z izotopů a sečteme je. Takže pro první hmotnost vynásobíme 0,50 % z 84 (amu - jednotky atomové hmotnosti) = 0,042 amu a přičteme to k 9,9 % z 86 amu = 8,51 amu atd
Jaký je rozdíl mezi hmotností protonu a hmotností elektronu?
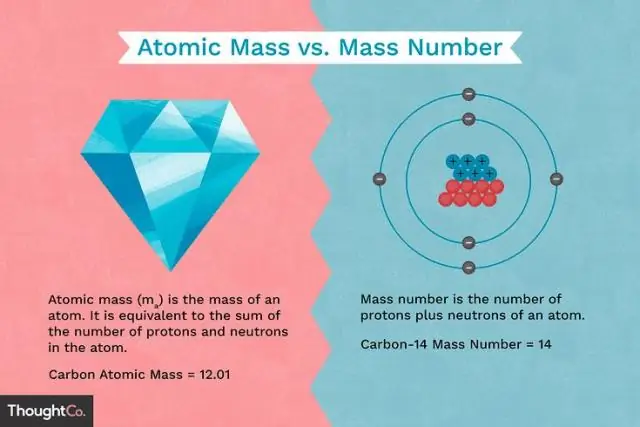
Protony a neutrony mají přibližně stejnou hmotnost, ale oba jsou mnohem hmotnější než elektrony (přibližně 2000krát hmotnější než elektron). Kladný náboj na protonu je co do velikosti stejný jako záporný náboj na elektronu
Jak vypočítáte atomovou hmotnost boru?
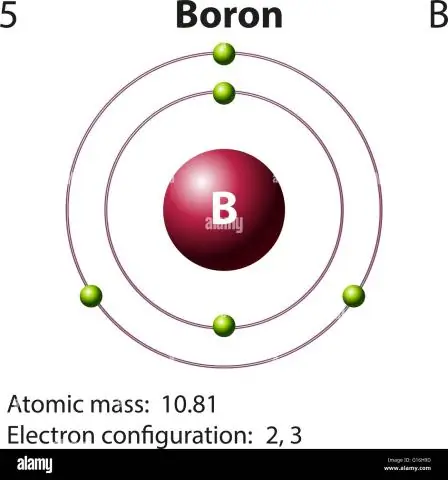
Pro bór bude tato rovnice vypadat takto: 5 protonů + 5 neutronů = 10 atomových hmotnostních jednotek (AMU) nebo pro častěji se vyskytující izotop boru (cca 5 protonů + 6 neutronů = 11 AMU
Jak řešíte problémy s omezenou hmotností reaktantů?

Najděte limitující činidlo výpočtem a porovnáním množství produktu, které každý reaktant vyprodukuje. Vyvažte chemickou rovnici pro chemickou reakci. Převeďte uvedené informace na krtky. Pro zjištění hmotnosti vyrobeného produktu použijte stechiometrii pro každý jednotlivý reaktant
Jak vypočítáte atomovou ekonomiku?
Obecný způsob, jak postupovat při výpočtu atomové ekonomiky, je použít následující kroky: Sestrojte chemickou rovnici pro danou reakci. Vyrovnejte rovnici. Vypočítejte hmotnosti reaktantů a produktů pomocí atomových hmotností a vzorce hmotnosti z periodické tabulky. Vypočítejte procentuální atomovou ekonomiku
