
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- Naposledy změněno 2025-01-22 16:56.
stříbrný je druhý prvek v jedenáctém sloupci periodické tabulky. Atomy stříbra mají 47 elektronů a 47 protonů s 60 neutrony v nejhojnějším izotopu. Charakteristika a vlastnosti. Za standardních podmínek stříbrný je měkký kov, který má lesklý kovový povrch.
Dále, k čemu se používá prvek stříbro?
to je používá šperky a stříbrný nádobí, kde je důležitý vzhled. stříbrný je použitý vyrábět zrcadla, protože je to nejlepší známý reflektor viditelného světla, i když časem zaniká. Je to také použitý v dentálních slitinách, pájecích a pájecích slitinách, elektrických kontaktech a bateriích.
Víte také, jak se v zemi tvoří stříbro? V rámci Země , stříbrný je vytvořený ze sloučenin síry. V Země kůra, teplota je velmi horká (přibližně 200 až 400 stupňů Fahrenheita, v závislosti na tom, jak blízko jste k plášti planety). Slaná voda, která existuje v kůře, se koncentruje do solného roztoku, kde stříbrný zůstává rozpuštěný.
Také je třeba vědět, jaké je atomové číslo stříbra?
47
Jak se jmenoval člověk, který objevil stříbro?
Otázky a odpovědi
| Název prvku | Discovered By | Rok |
|---|---|---|
| stříbrný | Známý od starověku | ? |
| Sodík | Sir Humphry Davy | 1807 |
| Stroncium | Adair Crawfordová | 1790 |
| Síra | Známý od starověku | ? |
Doporučuje:
Jaké jsou některé chemické vlastnosti stříbra?

Chemické vlastnosti stříbra - Účinky stříbra na zdraví - Účinky stříbra na životní prostředí Atomové číslo 47 Atomová hmotnost 107,87 g.mol -1 Elektronegativita dle Paulinga 1,9 Hustota 10,5 g.cm-3 při 20°C Bod tání 962 °C
Jaká je hmotnost 1 gramu atomu stříbra?

Znamená to: Hmotnost jednoatomového prvku v gramech, která bude obsahovat 1 mol jeho atomů. Rovná se atomové hmotnosti prvku, ale pouze se píše s příponou gramy. Pro např. Atomová hmotnost stříbra nebo atomová hmotnost 107,8682, takže jeho atomová hmotnost v gramu je 107,8682 gm
Jaká je úplná elektronová konfigurace základního stavu pro atom galia?

Základní elektronová konfigurace základního plynného neutrálního gallia je [Ar]. 3d10. 4s2. 4p1 a termínový symbol je 2P1/2
Jaký typ iontu vzniká, když atom ztratí elektron?
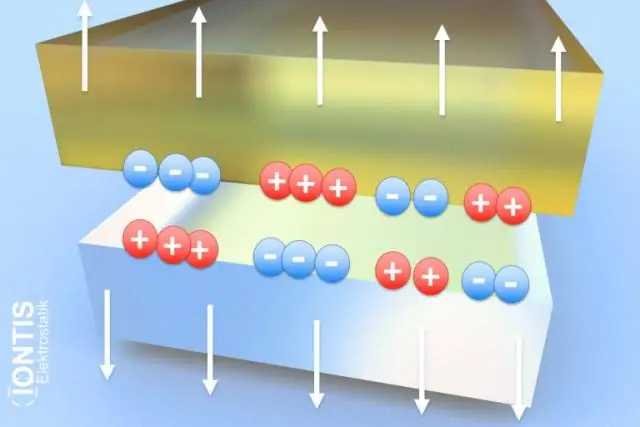
Ionty se tvoří, když atomy ztrácejí nebo získávají elektrony, aby splnily pravidlo oktetu a měly plné vnější valenční elektronové obaly. Když ztratí elektrony, stanou se kladně nabitými a nazývají se kationty. Když získají elektrony, jsou záporně nabité a nazývají se anionty
Jaká je základní elektronová konfigurace atomu stříbra?

Základní elektronová konfigurace základního plynného neutrálního stříbra je [Kr]. 4d10. 5s1 a termínový symbol je 2S1/2
