
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- Naposledy změněno 2025-01-22 16:56.
An iontová sloučenina je obr struktura z ionty . The ionty mají pravidelné, opakující se uspořádání zvané an iontová mřížka . Tento je proč pevný iontové sloučeniny tvoří krystaly pravidelných tvarů.
Kromě toho, proč existují iontové sloučeniny v krystalické mřížce?
Vlastnosti iontové sloučeniny vycházet z pořadí krystalová mřížka uspořádání pevně vázaných nabitých částic, které je tvoří. Iontové sloučeniny mají tendenci mít vysoké body tání a varu, protože mezi nimi je přitažlivost ionty v mříž je velmi silný.
Podobně, co je iontová mřížka? An iontový sloučenina se skládá z kationtů a aniontů a mříž struktura. The iontová mřížka struktura je držena pohromadě elektrostatickými přitažlivými silami mezi opačně nabitými ionty . Kov nebo kovová slitina se skládá z kovových kationtů a moře delokalizovaných elektronů.
Jsou všechny iontové sloučeniny krystalické?
Individuální ionty v rámci an iontová sloučenina mají obvykle více nejbližších sousedů, takže nejsou považovány za součást molekul, ale za součást souvislé trojrozměrné sítě, obvykle v krystalický struktura. Iontové sloučeniny typicky mají vysoké teploty tání a varu a jsou tvrdé a křehké.
Jaké jsou 4 vlastnosti iontových sloučenin?
Zde je krátký seznam hlavních vlastností:
- Tvoří krystaly.
- Mají vyšší entalpie fúze a odpařování než molekulární sloučeniny.
- Jsou těžké.
- Jsou křehké.
- Mají vysoké teploty tání a také vysoké teploty varu.
- Vedou elektřinu, ale pouze když jsou rozpuštěny ve vodě.
Doporučuje:
Jaký je příklad iontové sloučeniny?

Iontové sloučeniny jsou sloučeniny skládající se z iontů. Dvouprvkové sloučeniny jsou obvykle iontové, když jeden prvek je kov a druhý nekov. Příklady zahrnují: chlorid sodný: NaCl s ionty Na+ a Cl-. oxid hořečnatý: MgO s ionty Mg2+ a O2
Jaké jsou strukturní jednotky, které tvoří iontové sloučeniny a jak se nazývají?

U binárních iontových sloučenin (iontové sloučeniny, které obsahují pouze dva typy prvků) se sloučeniny pojmenovávají tak, že se nejprve napíše název kationtu a za ním název aniontu. Například KCl, iontová sloučenina, která obsahuje ionty K+ a Cl-, se nazývá chlorid draselný
Proč se iontové sloučeniny snadno rozpouštějí ve vodě?

K rozpuštění iontové sloučeniny musí být molekuly vody schopny stabilizovat ionty, které jsou výsledkem porušení iontové vazby. Dělají to hydratací iontů. Voda je polární molekula. Když umístíte iontovou látku do vody, molekuly vody přitahují kladné a záporné ionty z krystalu
Při pojmenování iontové sloučeniny typu 1 Jak pojmenujete kovový iont?

Iontové sloučeniny jsou neutrální sloučeniny tvořené kladně nabitými ionty nazývanými kationty a záporně nabitými ionty nazývanými anionty. U binárních iontových sloučenin (iontové sloučeniny, které obsahují pouze dva typy prvků) se sloučeniny pojmenovávají tak, že se nejprve napíše název kationtu a poté název aniontu
Jak píšete vzorce pro binární iontové sloučeniny?
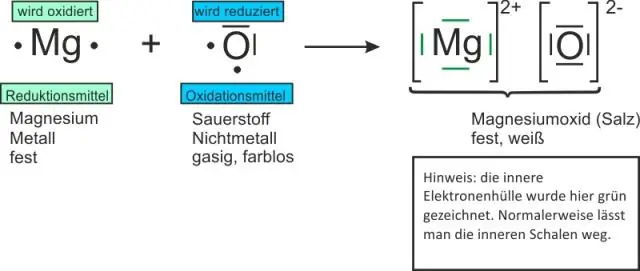
Vzorce pro binární sloučeniny začínají kovem, po kterém následuje nekov. Kladné a záporné náboje se musí navzájem rušit. Vzorce iontových sloučenin jsou zapsány s použitím nejnižšího poměru iontů
