Obsah:
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- Naposledy změněno 2025-01-22 16:56.
Molekulární vzorce řekne vám, kolik atomů každého prvku je ve sloučenině, a empirické vzorce řeknou vám nejjednodušší nebo nejvíce snížený poměr prvků ve sloučenině. Pokud je sloučenina molekulární vzorec již nelze snížit, pak empirický vzorec je stejný jako molekulární vzorec.
Jednoduše tedy, jak zjistíte molekulární vzorec z empirického vzorce?
Vydělte molární hmotnost sloučeniny empirický vzorec Hmotnost. Výsledkem by mělo být celé číslo nebo velmi blízké celému číslu. Vynásobte všechny indexy v empirický vzorec o celé číslo nalezené v kroku 2. Výsledkem je molekulární vzorec.
jaký je empirický vzorec sloučeniny, jejíž molekulový vzorec je s6o9? pokud molekulový vzorec je S6O9 získat empirický vzorec hledáme číslo, které bude dělit na 6 a 9 až pět nejmenší poměr celých čísel (což je definice empirický vzorec !).
Jednoduše tedy, jak zjistíte molekulový vzorec z empirického vzorce a molární hmotnosti?
Empirický vzorec hmotnost = (1 x 12,01 g/mol) + (2 x 1,01 g/mol) + (1 x 16,00 g/mol) = 30,02 g/mol. Rozdělit molární hmotnost pro molekulární vzorec podle empirický vzorec hmotnost . Výsledek určuje, kolikrát se mají vynásobit indexy v empirický vzorec získat molekulární vzorec.
Jak řešíte empirický vzorec?
Výpočet empirického vzorce
- Krok 1: Zjistěte hmotnost každého přítomného prvku v gramech. % prvku = hmotnost vg = m.
- Krok 2: Určete počet molů každého typu přítomného atomu.
- Krok 3: Vydělte počet molů každého prvku nejmenším počtem molů.
- Krok 4: Převeďte čísla na celá čísla.
Doporučuje:
Proč je empirický vzorec oxidu hořečnatého MgO?

Empirický vzorec pro oxid hořečnatý je MgO. Hořčík je kationt +2 a oxid je aniont -2. Protože náboje jsou stejné a opačné, tyto dva ionty se spojí v poměru 1:1 atomů
Jaký je empirický vzorec oktanu?

C8H18 Jaký je zde empirický vzorec oktanu c8h18? The empirický vzorec oktanu $$C_{8}H_{18}$$ je: A. B C. Podobně, jaký je empirický vzorec c2h6o2? Molekulární a empirické vzorce Otázka Odpovědět Napište empirický vzorec pro následující sloučeninu:
Jak zjistíte empirický vzorec s procenty?

Přepis Vydělte každé % atomovou hmotností prvku. Vydělte každou z TĚCH odpovědí podle toho, co je nejmenší. Upravte tato čísla na nejnižší poměr celých čísel
Jaký je empirický vzorec pro kofein?
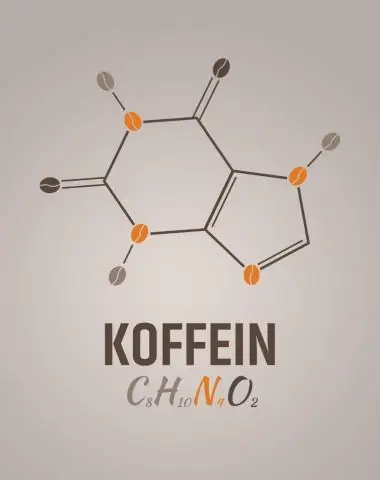
2 Odpovědi. C8H10N4O2 je molekulární vzorec pro kofein
Jaký je empirický vzorec pro bromid strontnatý?

SrBr2 Jaký je tedy vzorec pro bromid strontnatý? SrBr2 Navíc je bromid strontnatý vodný? O Bromid strontnatý Hexahydrát Lze uvažovat o ultra vysoké čistotě, vysoké čistotě, submikronové a nanopráškové formě. Většina kovových bromid sloučeniny jsou rozpustné ve vodě.
