
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- Naposledy změněno 2025-01-22 16:56.
Slabý elektrolyty jsou látky, které po rozpuštění ve vodě disociují na ionty jen částečně. Slabé kyseliny, jako je kyselina octová, nacházející se v ocet a slabé báze, jako je amoniak, nacházející se v čisticích prostředcích, jsou příklady slabých elektrolyty . Cukr je klasifikován jako a neelektrolyt.
Lidé se také ptají, je cukr elektrolyt nebo neelektrolyt?
Iontově vázané látky působí jako elektrolyty. Ale kovalentně vázané sloučeniny, ve kterých ne ionty jsou přítomny, jsou běžně neelektrolyty. Stolní cukr nebo sacharóza , je dobrým příkladem neelektrolytu. Cukr můžete rozpustit ve vodě nebo roztavit, ale nebude mít vodivost.
Podobně, co popisuje elektrolyt? An elektrolyt je látka, která po rozpuštění v polárním rozpouštědle, jako je voda, vytváří elektricky vodivý roztok. Příklady jsou sodík, draslík, chlorid, vápník, hořčík a fosforečnan elektrolyty.
Vzhledem k tomu, je hno3 elektrolyt nebo neelektrolyt?
Iontové sloučeniny jsou pravděpodobněji silné elektrolyty . Silné kyseliny jsou také silné elektrolyty . Sloučeniny, které jsou tvořeny z prvků skupiny 17, jako je HCl, HBr a HI, jsou silné kyseliny. Mezi další silné kyseliny patří H2SO4, HNO3 HC103 a HC104.
Je HCl neelektrolyt?
Chlorovodík ( HCl ) je plyn v čistém molekulárním stavu a je a neelektrolyt . Když HCl se rozpustí ve vodě, tzv kyselina chlorovodíková . Iontové sloučeniny a některé polární sloučeniny jsou zcela rozbity na ionty a tak velmi dobře vedou proud.
Doporučuje:
Co je na prvním místě délka nebo šířka nebo výška?
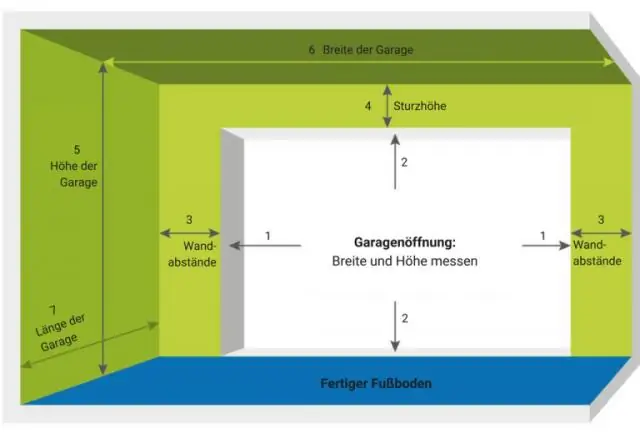
Co je první? Průmyslový standard grafiky je šířka na výšku (šířka x výška). To znamená, že když píšete své míry, píšete je ze svého pohledu, počínaje šířkou. To je důležité
Je berylium kov nebo nekov nebo metaloid?

Berylium je kov. Je ve skupině kovů alkalických zemin v periodické tabulce a má chemické a fyzikální vlastnosti podobné vlastnostem hořčíku a hliníku, ale má výrazně vyšší bod tání než oba
Je uhlík kov nebo nekov nebo metaloid?

Uhlík má ve svém valenčním obalu 4 elektrony, což z něj dělá metaloid, ale běžně je považován za nekov
Je kujný kov nebo nekov nebo metaloid?

Kovy, metaloidy a nekovy. Prvky mohou být klasifikovány jako kovy, nekovy nebo metaloidy. Kovy jsou dobrými vodiči tepla a elektřiny a jsou kujné (lze je zatlouct do plechů) a tažné (lze je vtáhnout do drátu). Metaloidy jsou svými vlastnostmi střední
Je ocet polární nebo nepolární?

Kyselina octová a voda jsou polární molekuly. Stejně tak nepolární molekuly preferují být obklopeny jinými nepolárními molekulami. Když se polární roztok, jako je ocet, intenzivně smíchá s nepolárním roztokem, jako je olej, oba zpočátku vytvoří emulzi, směs polárních a nepolárních sloučenin
