
Obsah:
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- Naposledy změněno 2025-01-22 16:56.
Buffer
- Pokud máte jen slabé kyselina . Určete koncentraci kyselina (za předpokladu, že nedochází k disociaci). Vyhledejte nebo určete KA.
- Pokud máte slabé kyselina A konjugát základna . Řešit pro vyrovnávací paměť.
- Pokud máte pouze konjugát základna . Řešit pro pH základna pomocí Kb a rovnice hydrolýzy.
Jak tedy provádíte acidobazickou titraci?
Postup titrace
- Propláchněte byretu standardním roztokem, pipetu neznámým roztokem a kuželovou baňku destilovanou vodou.
- Pomocí pipety vložte přesně odměřený objem analytu do Erlenmeyerovy baňky spolu s několika kapkami indikátoru.
Podobně, jak vypočítáte titraci? Použijte titrační vzorec . Pokud mají titrační činidlo a analyt molární poměr 1:1, vzorec je molarita (M) kyseliny x objem (V) kyseliny = molarita (M) báze x objem (V) báze. ( Molarita je koncentrace roztoku vyjádřeného jako počet molů rozpuštěné látky na litr roztoku.)
Kromě toho je F silná nebo slabá základna?
Proto jsem- je nejstabilnější a nejméně základní F - je nejméně stabilní a nejzákladnější. Silné základy zcela interagovat s silný kyseliny jako HCl za vzniku soli a vody v neutralizační reakci. jiný silné základy jsou rozpustné oxidy, jako je Na2O a rozpustné hydroxidové soli. Silné základy jsou silný elektrolyty.
K čemu se titrace používá?
A titrace je technika, kde je roztok o známé koncentraci zvyklý určit koncentraci neznámého roztoku. Typicky se titrační činidlo (známý roztok) přidává z byrety ke známému množství analytu (neznámý roztok), dokud není reakce dokončena.
Doporučuje:
Jaké jsou kroky k řešení slovních úloh?
Jednoduché kroky pro řešení problémů se slovem Přečtěte si problém. Začněte pozorným přečtením problému. Identifikujte a vyjmenujte fakta. Zjistěte, co přesně problém vyžaduje. Odstraňte přebytečné informace. Věnujte pozornost měrným jednotkám. Nakreslete schéma. Najděte nebo vytvořte vzorec. Poraďte se s odkazem
Jaké jsou kroky k řešení dvoukrokových nerovností?

Řešení rovnice nebo nerovnosti, která má více než jednu operaci, vyžaduje dva kroky: Zjednodušte pomocí inverze sčítání nebo odčítání. Dále zjednodušte pomocí inverzní funkce násobení nebo dělení
Jaké jsou kroky při násobení racionálního algebraického výrazu?
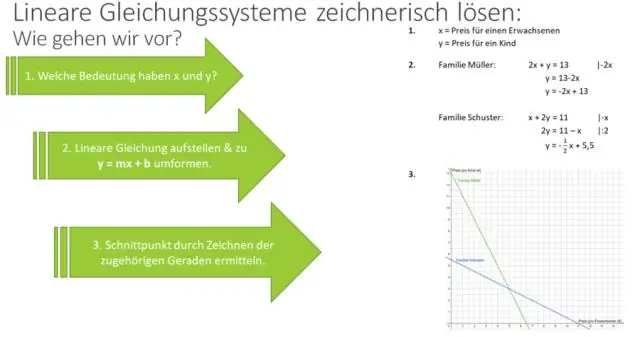
Q a S se nerovnají 0. Krok 1: Faktor čitatele i jmenovatele. Krok 2: Napište jako jeden zlomek. Krok 3: Zjednodušte racionální vyjádření. Krok 4: Vynásobte zbývající faktory v čitateli a/nebo jmenovateli. Krok 1: Faktorujte čitatel i jmenovatel. Krok 2: Napište jako jeden zlomek
Jaké jsou kroky při použití volumetrické pipety?

Použití volumetrické pipety Pipetu dvakrát nebo třikrát vypláchněte kapalinou, kterou chcete přenést. Pokud jste pravák, umístěte pipetu do pravé ruky a pipetovou baňku do levé (leváci dělají opak). Stiskněte baňku a umístěte ji přes konec pipety
Jaké jsou kroky řešení rovnice?

Chcete-li vyřešit dvoukrokovou algebraickou rovnici, vše, co musíte udělat, je izolovat proměnnou pomocí sčítání, odčítání, násobení nebo dělení. Vyřešte dvoukrokovou rovnici tak, že na konci místo dělení vynásobíte. x/5 + 7 = -3 = (x/5 + 7) - 7 = -3 - 7 = x/5 = -10. x/5 * 5 = -10 * 5. x = -50
