
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- Naposledy změněno 2025-01-22 16:56.
Zákon ideálního plynu, jak se říká, ve skutečnosti je PV = nRT , se všemi standardními proměnnými. Zde n=m/M, kde m je hmotnost plynu a M je molekulová hmotnost plynu. Zkrátka R in PV = nRT je zmenšena o faktor M (molekulová hmotnost), aby se dostalo R PV = mr T.
Jednoduše řečeno, čemu se r rovná v pV nRT?
Ideální zákon o plynu je: pV = nRT , kde n je počet molů a R je univerzální plynová konstanta. Hodnota R závisí na zúčastněných jednotkách, ale obvykle se u jednotek S. I. uvádí jako: R = 8,314 J/mol. To znamená, že pro vzduch můžete použít hodnotu R = 287 J/kg.
Podobně, co znamená R v chemii pV nRT? Jednotky univerzální plynové konstanty R je odvozeno z rovnice PV=n R T To stojí pro Regnault.
Co v tomto ohledu znamená N v pV nRT?
. Fyzikální zákon popisující vztah měřitelných vlastností ideálního plynu, kde P (tlak) × V (objem) = (počet molů) × R (plynová konstanta) × T (teplota v Kelvinech). Je odvozen z kombinace zákonů o plynech Boyla, Charlese a Avogadra. Také se nazývá univerzální zákon o plynu.
Co je M v zákoně ideálního plynu?
Originál zákon o ideálním plynu používá vzorec PV =nRT, verzi hustoty zákon o ideálním plynu je PM = dRT, kde P je tlak měřený v atmosférách (atm), T je teplota měřená v kelvinech (K), R je zákon o ideálním plynu konstantní 0,0821 at m (L) m ol(K) stejně jako v původním vzorci, ale M je nyní molární hmotnost (g m ol
Doporučuje:
Jaký je rozdíl mezi osmózovou difuzí a usnadněnou difuzí?

Osmóza také nastává, když se voda pohybuje z jedné buňky do druhé. Usnadněná difúze na druhé straně nastává, když médium obklopující buňku má vysokou koncentraci iontů nebo molekul než prostředí uvnitř buňky. Molekuly se pohybují z okolního prostředí do buňky díky difúznímu gradientu
Jaký je rozdíl mezi korelací a chi kvadrátem?
Korelace je tedy o lineárním vztahu mezi dvěma proměnnými. Obvykle jsou oba spojité (nebo téměř tak), ale existují varianty pro případ, kdy je jeden dichotomický. Chí-kvadrát je obvykle o nezávislosti dvou proměnných. Obvykle je obojí kategorické
Jaký je rozdíl mezi klimatickým pásmem a biomem?

Klima je klasifikováno na základě atmosférické teploty a srážek, zatímco biom je klasifikován především na základě jednotných typů vegetace. Klima může určit, jaký biom je přítomen, ale biom obvykle neřídí ani neovlivňuje klima stejným způsobem
Jaký je rozdíl mezi tvrdým a měkkým osvětlením?

Rozdíl mezi měkkým světlem a tvrdým světlem. Tvrdé světlo vytváří výrazné stíny s ostrými hranami. Měkké světlo vytváří stíny, které jsou sotva viditelné. Slunečný den je tvrdé světlo
Jaký je rozdíl mezi obecnou chemií a organickou chemií?
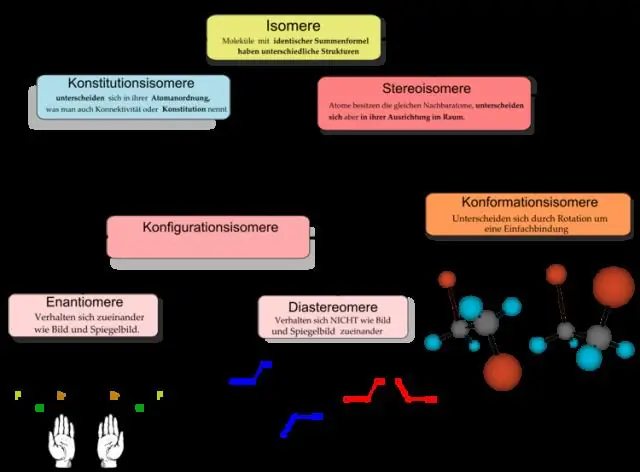
Organická chemie je považována za podobor chemie. Zatímco obecný zastřešující termín „chemie“se týká složení a přeměn veškeré hmoty obecně, organická chemie je omezena na studium pouze organických sloučenin
