
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- Naposledy změněno 2025-01-22 16:56.
Ten chlór izotop s 18 neutrony má hojnost 0,7577 a hmotnostní číslo 35 amu. Pro výpočet průměrný atomovou hmotnost, vynásobte zlomek číslem hmotnosti pro každý izotop a poté je přidejte dohromady.
Podobně, jaký je vážený průměr všech izotopů prvku?
Pomocí mas různých izotopy a jak je každý bohatý izotop je, můžeme najít průměrný hmotnost atomů an živel . Atomová hmotnost an živel je vážený průměr hmotnost atomů v přirozeně se vyskytujícím vzorku živel . Atomová hmotnost se obvykle uvádí v jednotkách atomové hmotnosti.
co má hmotnost 1 amu? Atomová hmotnostní jednotka (symbolizovaná AMU nebo amu) je definována jako přesně 1/12 hmotnosti atomu uhlíku-12. Atom uhlíku-12 (C-12) má šest protony a šest neutrony v jeho jádru. Nepřesně řečeno, jedna AMU je průměrem proton odpočinková hmota a neutron odpočinková mše.
Za druhé, jak vypočítáte procento výskytu pomocí atomové hmotnosti?
Změňte každý procentuální hojnost do desítkové formy vydělením 100. Vynásobte tuto hodnotu číslem atomová hmotnost toho izotopu. Sečtěte pro každý izotop, abyste získali průměr atomová hmotnost.
Jaký je rozdíl mezi atomovou hmotností a atomovou hmotností?
Atomová hmotnost (mA) je Hmotnost z an atom . Jediný atom má stanovený počet protonů a neutronů, takže Hmotnost je jednoznačný (nemění se) a je součtem počtu protonů a neutronů v atomu . Atomová hmotnost je váženým průměrem Hmotnost ze všech atomy prvku na základě množství izotopů.
Doporučuje:
Jak interpretujete vážený průměr?

Souhrn. Vážený průměr: Průměr, kdy některé hodnoty přispívají více než jiné. Když se váhy sečtou k 1: stačí vynásobit každou váhu odpovídající hodnotou a vše sečíst. V opačném případě vynásobte každou váhu w její odpovídající hodnotou x, sečtěte vše a vydělte součtem vah: Vážený průměr = ΣwxΣw
Jak zjistíte chybějící číslo, když je uveden průměr?

Průměr množiny čísel je průměr těchto čísel. Průměr najdete sečtením sady čísel a dělením, kolika čísel je dáno. Pokud dostanete průměr a požádáte o nalezení chybějícího čísla ze sady, použijte jednoduchou rovnici
Jak vytvoříte vážený průměr v kontingenční tabulce?

Vážené průměry v kontingenční tabulce Klepněte na šipku dolů vedle slova kontingenční tabulka na levé straně panelu nástrojů kontingenční tabulky. Vyberte Vzorce | Vypočítaná pole. Do pole Název zadejte název nového pole. Do pole Vzorec zadejte vzorec, který chcete použít pro váš vážený průměr, například =VáženáHodnota/Hmotnost. Klepněte na tlačítko OK
Jak zjistíte plochu, když je uveden průměr?

Chcete-li najít plochu kruhu s poloměrem, umocněte poloměr nebo jej vynásobte samotným. Potom vynásobte druhý poloměr číslem pí neboli 3,14, abyste získali plochu. Chcete-li najít oblast s průměrem, jednoduše vydělte průměr 2, vložte jej do vzorce pro poloměr a vyřešte jako dříve
Jak zjistíte průměr a medián v obraze?
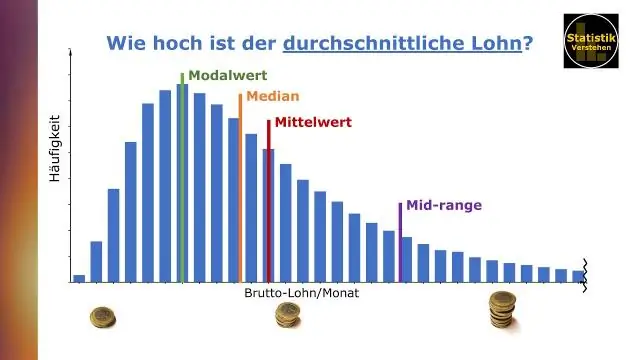
Komunikace dat s Tableau od Bena Jonese Průměr (neboli průměr) je určen sečtením všech hodnot v souboru dat a dělením počtem hodnot. Medián je střední hodnota v sadě dat, ve které byly hodnoty uspořádány podle velikosti
